ヒトを含む哺乳類の脳には1千億個ともされるニューロンが存在しています。これらのニューロンが決められた発生プログラムにしたがって正しく接続することで、運動・感覚・情動などの非常に多岐にわたる脳機能を司る精巧な神経回路網がつくられます。本研究室では、この神経回路網を構築するしくみを明らかにすること、そして、この異常によって起こる疾患のしくみを解明することを目指しています。また、神経機能が徐々に低下していく脳の老化機構の解明にも取り組んでいます。
<ニューロンの機能的な“かたちづくり”のメカニズム>
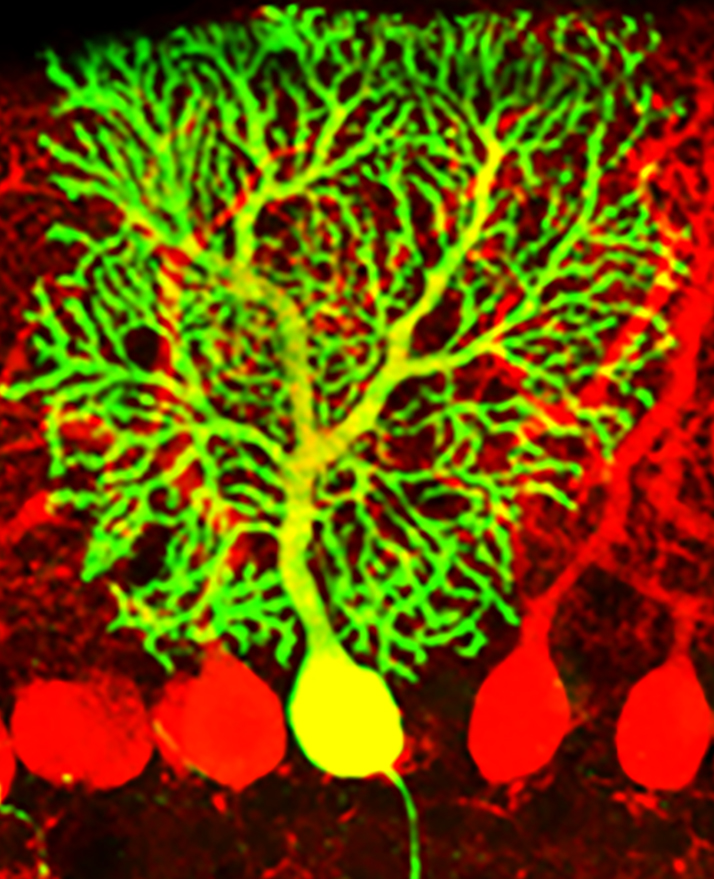
ニューロンの最大の特徴は2つの神経突起、つまり、“情報”の入力装置である「樹状突起」と出力装置である「軸索」をもつことです。これらの神経突起が空間的に正しく配置されることで、適切な回路接続がつくられます。特に、樹状突起のかたちはニューロンのタイプごとに大きく異なり、入力線維の種類やニューロンの情報処理能力を規定する大きな要因となります。つまり、個々のニューロンのかたちには機能に直結する重要な意味があるのです。わたしたちは、精巧な三次元構造の樹状突起をもつ小脳プルキンエ細胞をモデルとして、その樹状突起の空間配置のしくみを研究してきました。そして、まず、リン酸化酵素LKB1シグナル経路が、自己の樹状突起どうしの交錯を防ぐ重要なはたらきをしていることを明らかにしました(Cell Reports, 2018; Front Mol Neurosci, 2018)。また、プルキンエ細胞の特徴である大きな1本の樹状突起を構築するためにアクチン骨格制御因子N-WASP-Arp2/3シグナルが必須であることも明らかにしました(Development, 2022)。プルキンエ細胞を含む多くのニューロンの樹状突起にはそれぞれ固有の特徴がありますが、それらの制御システムはいまだによくわかっていません。わたしたちは、樹状突起のかたちづくりの基本原理を明らかにし、その機能的な意味に迫ることを目指しています。
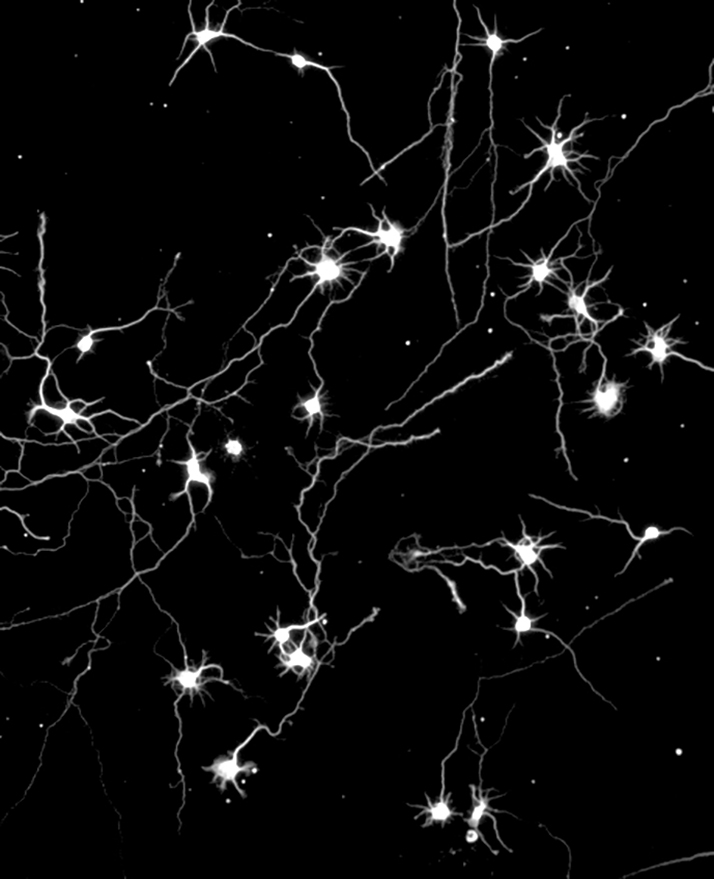
特定の神経回路接続が構築されるまでには、発生期の多くのステップをすべて正しく経る必要があります。特に、軸索を遠く離れた標的の領域まで正しく導く「軸索誘導」、そして、そのあと特定の標的細胞を正しく認識してシナプスをつくる「特異的シナプス結合」はどちらも神経回路の接続特異性を決定する上で欠かせない重要なステップです。わたしたちは、後脳ニューロンの発生過程において軸索誘導因子受容体Robo3のRNAレベルでの発現制御が非常に大きな役割を担っていることを明らかにし、軸索誘導機構におけるRNA制御の重要性を世界で初めて示しました(Neuron, 2010)。また、同じく後脳ニューロンの特異的シナプス結合を担う分子としてシナプス接着因子Cadherin-7を発見し、その発現を抑制すると回路の接続特異性が失われて混線が起こることを明らかにしました(Cell Reports, 2014)。このような回路形成で重要なはたらきをする軸索誘導因子群やシナプス接着因子群がそれぞれのニューロンで時間的・空間的に特異的な発現パターンを獲得することでニューロンごとに固有の回路接続が確立されます。つまり、その遺伝子発現プログラムこそが脳神経回路の接続パターンを規定する「脳の設計図」となるわけです。わたしたちは、いまだほとんど明らかにされていないこの遺伝子発現プログラムを紐解いていきます。
<生理的な脳老化を引き起こすメカニズム>

脳が正しく機能し続けるためには、ニューロンがその正常な神経活動を長期にわたって維持する必要があります。生理的な脳の老化では、このニューロンの機能が徐々に低下することで脳機能の衰退が起こるとされていますが、その分子基盤はいまだにほとんどわかっていません。私たちは、最近、神経活動を制御するまったく新しいシステムを発見し、その破綻が脳の老化に関わる可能性を明らかにしました。現在は、詳細なメカニズムの解明とそれに基づいた抗脳老化戦略の開発に取り組んでいます(AMED-PRIME「根本的な老化メカニズムの理解と破綻に伴う疾患機序解明」令和5年度採択)。
